Trong công nghiệp, từ khí SO2 và O2, phản ứng hóa học tạo thành SO3 xảy ra ở điều kiện nào sau đây
A. Nhiệt độ phòng và có mặt xúc tác V2O5
B. Đun nóng đến 500 o C và có xúc tác V2O5
C. Đun nóng đến 500 o C
D. Nhiệt độ phòng
Biện pháp nào làm tăng hiệu suất tổng hợp SO3 từ SO2 và O2 trong công nghiệp ? Biết phản ứng tỏa nhiệt.
(a) Thay O2 không khí bằng O2 tinh khiết.
(b) Tăng áp suất bằng cách nén hỗn hợp.
(c) Thêm xúc tác V2O5.
(d) Tăng nhiệt độ để tốc độ phản ứng
A. (b), (c).
B. (a), (b).
C. (a).
D. (a), (b), (c), (d).
Chọn B
Thay O2 không khí bằng O2 tinh khiết là làm tăng nồng độ của O2. Trường hợp này cân bằng chuyển dịch theo chiều thuận, do đó làm tăng hiệu suất của phản ứng.
Tăng áp suất thì cân bằng hóa học sẽ chuyển dịch theo chiều làm giảm số phân tử khí, tức là chiều thuận, do đó cũng làm tăng hiệu suất tổng hợp SO3.
Chất xúc tác không làm ảnh hưởng đến sự chuyển dịch cân bằng, nó chỉ giúp cho cân bằng nhanh chóng được thiết lập.
Tăng nhiệt độ thì cân bằng sẽ chuyển dịch theo chiều thu nhiệt, tức là chiều nghịch, do đó làm giảm hiệu suất phản ứng.
Vậy các biện pháp (a) và (b) là tăng hiệu suất phản ứng
Trong một bình kín chứa 2 mol O2, 3 mol SO2 và một ít bột xúc tác V2O5. Nung nóng bình một thời gian thu được hỗn hợp khí B.
SO2 + O2 -----V2O5,to----->SO3
1. Nếu hiệu suất phản ứng oxi hóa SO2 thành SO3 là 75% thì có bao nhiêu mol SO3 tạo thành?
2. Nếu tổng số mol các khí trong B là 4,25. Hãy tính hiệu suất phản ứng oxi hóa SO2 thành SO3
1)
Xét tỉ lệ: \(\dfrac{3}{2}< \dfrac{2}{1}\) => Hiệu suất tính theo SO2
\(n_{SO_2\left(pư\right)}=\dfrac{3.75}{100}=2,25\left(mol\right)\)
PTHH: 2SO2 + O2 -----V2O5,to-----> 2SO3
2,25--------------------->2,25
=> nSO3 = 2,25 (mol)
2) Gọi số mol SO2 pư là a (mol)
PTHH: 2SO2 + O2 -----V2O5,to-----> 2SO3
Trc pư: 3 2 0
Pư: a-->0,5a-------------------->a
Sau pư: (3-a) (2-0,5a) a
=> (3-a) + (2-0,5a) + a = 4,25
=> a = 1,5 (mol)
=> \(H=\dfrac{1,5}{3}.100\%=50\%\)
Trong 1 bình kín chứa 4,48 lít oxi và 6,72 lít khí SO2 và một ít xúc tác V2O5. Nung nóng bình một thời gian xảy ra phản ứng theo sơ đồ sau:
O2 + SO2 ---------> SO3
a) Nếu hiệu suất là 90% thì có bao nhiêu lít khí SO3 tạo thành. Biết các khí do ở cùng điều kiện nhiệt độ và áp suất
b) Sục khí SO3 vào nước có sẵn mẫu quỳ tím. Nêu hiện tượng và viết phương trình hóa học xảy ra
a)
$2SO_2 + O_2 \xrightarrow{t^o,V_2O_5} 2SO_3$
Ta thấy :
V SO2 / 2 = 3,36 < V O2 / 1 = 4,48 nên hiệu suất tính theo số mol SO2
n SO2 = 6,72/22,4 = 0,3(mol)
n SO3 = n SO2 pư = 0,3.90% = 0,27(mol)
=> V SO3 = 0,27.22,4 = 6,048(lít)
b) Giấy quỳ tím chuyển dần sang màu đỏ :
$SO_3 + H_2O \to H_2SO_4$
a) \(PTHH:2SO_2+O_2\xrightarrow[V_2O_5]{450^oC}2SO_3\)
\(n_{SO_2}=\dfrac{32}{64}=0,5\left(mol\right)\\ n_{O_2}=\dfrac{10}{32}=0,3125\left(mol\right)\)
Lập tỉ lệ: \(\dfrac{n_{SO_2}}{2}< \dfrac{n_{O_2}}{1}\left(\dfrac{0,5}{2}< 0,3125\right)\)
=> SO2 hết O2 dư
Theo pt: \(n_{O_2\left(pư\right)}=\dfrac{n_{SO_2}.2}{3}=\dfrac{0,5.1}{2}=0,25\left(mol\right)\)
\(n_{O_2\left(dư\right)}=0,3125-0,25=0,0625\left(mol\right)\\ m_{O_2}=0,0625.32=2\left(g\right)\)
c) Theo pt, ta có:\(n_{SO_3}=n_{SO_2}=0,5\left(mol\right)\)
\(m_{SO_3}=0,5.80=40\left(g\right)\)
ở nhiệt độ cao và có xúc tác V2O5 thì khí lưu huỳnh đioxit hóa hợp với khí O2 tạo thành hợp chất Lưu huỳnh trioxit . Người ta trộn 0,5 mol SO2 với 0,4 mol O2 rồi thực hiện phản ứng sau một thơi gian thu được hỗn hợp khí Y , trong đó số mol chất ẩn phẩm chiếm 40% số mol hỗn hợp Y . Tính H% oxi hoá lưu huỳnh đioxit
Ở nhiệt độ phòng, hỗn hợp khí X gồm hiđrocacbon A và lượng dư hiđro có tỉ khối so với H2 là 3,375. Khi cho X qua Ni đun nóng cho đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Y có tỉ khối so với H2 là 4,5.
a) Xác định công thức phân tử của A.
b) Tính thành phần phần trăm theo thể tích của các chất có trong X.
Nếu cho X qua Pd/BaSO4 đun nóng cho đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Z. Trong Z chỉ có hai chất khí là B và hiđro.
c) Viết phương trình phản ứng tạo thành B trên. Tính tỉ khối của Z so với hiđro.
d) B có thể cho phản ứng polime hóa. Viết phương trình phản ứng này.
Hợp chất B cho phản ứng với Cl2 ở 500 tạo thành C (có chứa 46,4% khối lượng Cl). C phản ứng với dung dịch NaOH loãng thu được D. Cho D phản ứng với nước và Cl2 thu được E (có chứa 32,1% khối lượng Cl). Sau cùng E phản ứng với dung dịch NaOH loãng thu được F.
e) Viết công thức cấu tạo của các chất từ B đến F và viết các phương trình hóa học xảy ra
a.
BTKL ta có mX = mY => nX . MX = nY . mY
MX / My = nY / mY =0.75
Đặt nX = 1 mol => nY = 0,75 mol => nH2 phản ứng = 1 – 0,75 = 0,25mol
* TH hidrocacbon là anken: n anken = n H2 = 0,25 mol => n H2 trong X = 0,75 => M = (6,75 – 0,75 . 2)/0,25 = 21 (loại) * TH là ankin: => n akin = 0,25/2 = 0,125 => n H2 trong X = 0,875 mol => M = (6,75 – 0,875 . 2)/0,125 = 40 =>C3H4
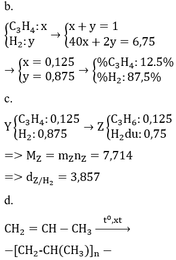

Cho 4,48 lít khí SO2 tác dụng với 2,24 lít khí O2. Thêm xúc tác và nung nóng cho phản ứng xảy ra. Sau khi phản ứng kết thúc, ta thu được 5,6 lít hỗn hợp khí gồm SO2, O2, SO3. Tính thể tích mỗi khí có trong hỗn hợp sau phản ứng và tính hiệu suất của phản ứng. Biết các khí đo ở đktc
Gọi hiệu suất phản ứng là a
$2SO_2 + O_2 \xrightarrow{t^o,V_2O_5} 2SO_3$
Ta thấy :
V SO2 / 2 = V O2 nên hiệu suất tính theo số mol của SO2 hoặc O2
V SO2 phản ứng = 4,48a(lít)
V O2 phản ứng = 2,24a(lít)
V SO3 = V SO2 pư = 4,48a(lít)
Sau phản ứng, khí gồm :
SO2 : 4,48 - 4,48a(lít)
O2 : 2,24 - 2,24a(lít)
SO3 : 4,48a(lít)
Suy ra :
4,48 - 4,48a + 2,24 - 2,24a + 4,48a = 5,6
=> a = 0,5 = 50%
Hỗn hợp khí gồm :
SO2 : 4,48 -4,48.0,5 = 2,24 lít
O2 : 2,24 - 2,24.0,5 = 1,12 lít
SO3 : 4,48.0,5 = 2,24 lít
Cho 6,4g SO2 tác dụng với 3,2g khí oxi ở nhiệt độ cao, có xúc tác V2O5. Sau phản ứng xảy ra hoàn toàn , hãy: a, xác định chất nào còn dư b, xác định khối lượng lưu huỳnh trioxit(SO3) thu được Mn giúp mk vs ạ , mai mk thi rồi. Thank cb nhiều
nSO2=0,1(mol); nO2=0,1(mol)
a) PTHH: 2 SO2 + O2 \(⇌\) 2 SO3 (xt: V2O5)
Ta có: 0,1/2 < 0,1/1
=> O2 dư, SO2 hết, tính theo nSO2.
b) nSO3=nSO2=0,1(mol)
=> mSO3=0,1.80=8(g)
Trong công nghiệp sản xuất H2SO4, giai đoạn oxi hóa SO2 thành SO3, được biểu diễn bằng phương trình phản ứng:
2 S O 2 ( K ) + O 2 ( K ) ⇆ V 2 O 5 , t o 2 S O 3 ( K ) , △ H < 0
Cân bằng hóa học sẽ chuyển dời về phía tạo ra sản phẩm là SO3, nếu
A. tăng nồng độ khí O2 và tăng áp suất
B. giảm nồng độ khí O2 và giảm áp suất
C. tăng nhiệt độ và giảm áp suất
D. giảm nhiệt độ và giảm nồng độ khí SO2
Cân bằng hóa học chuyển dời về phía tạo ra sản phẩm là SO3, có nghĩa cân bằng chuyển dịch về chiều thuận. Các yếu tố có thể làm điều đó là:
- Tăng nồng độ SO2 hoặc O2
- Giảm nồng độ SO3
- Tăng áp suất nt > ns
- Giảm nhiệt độ